- Азулен
-
Азулен 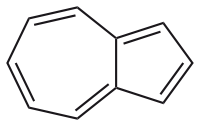
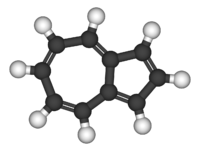
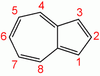
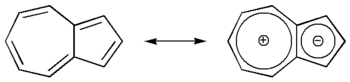
Общие Систематическое наименование Азулен Химическая формула С10Н8 Физические свойства Молярная масса 128,17 г/моль Термические свойства Температура плавления 99 °C Температура кипения 242 °C Классификация Рег. номер CAS 275-51-4 SMILES C1=CC=C2C=CC=C2C=C1 RTECS CO4570000 Азуле́н — С10Н8 — бицикло[5.3.0]декапентаен — небензоидное ароматическое соединение, содержащее конденсированную систему из 5- и 7-членного циклов. Является изомером нафталина. Молекула обладает дипольным моментом.
Вследствие высокой электронной плотности на 5-членном цикле, азулен обладает относительно высокой химической активностью, легко вступая в реакции с электрофильными агентами.
Содержание
История открытия
Азулен впервые был получен в 15 веке в виде синего красящего вещества, выделенного из эфирного масла ромашки. Тогда ему не придали значения, а вещество не идентифицировали. Вторично азулен был обнаружен в 1863 году французским парфюмером Септимусом Пьессом в тысячелистнике и полыни. Тогда же он и получил свое название. Открыл структуру азулена и осуществил его первый синтез швейцарский химик-органик Леопольд (Лавослав) Ружичка в 1937 году.
Нахождение в природе
Производные азулена достаточно широко встречаются в природных эфирных маслах[1]:
- Хамазулен 1,4-диметил-7-этилазулен: компонент эфирного масла из ромашки (Matricaria chamomilla L. syn. Matricaria recutita) и тысячелистника (Achillea millifolium L.).
- Гвайазулен 1,4-диметил-7-изопропилазулен: входит в состав эфирного масла некоторых эвкалиптов; выделяется из высококипящих фракций эфирного масла Eucalyptus globulus, гурьюн-бальзама, реюньонской герани, Geranium macrorrhizum и пачули.
- Изогвайазулен 2,4-диметил-7-изопропилазулен. Найден в эфирном масле тысячелистника (Achillea millefolium).
Физические свойства
Кристаллическое вещество синего или сине-фиолетового цвета. Нерастворим в воде, растворим в углеводородах, диэтиловом эфире, этаноле. Перегоняется с паром[2].
Хорошо растворяется в серной и фосфорной кислоте с образованием солей (при этом его синяя окраска исчезает). Легко образует π-комплексы с пикриновой кислотой и тринитробензолом.
Химические свойства
- При нагревании свыше 300 °C изомеризуется в нафталин.
- Постепенно окисляется кислородом воздуха, а при действии KMnO4 в кислой среде расщепляется до смеси жидких и газообразных продуктов.
- В реакциях электрофильного и радикального замещения ведет себя подобно высокоактивным пятичленным гетероциклам.
Относительно легко нитруется тетранитрометаном в среде пиридина:

В реакциях галогенирования, ацилирования, азосочетания и др. замещение идет в положение 1 и затем 3:

- В реакциях с нуклеофилами азулен менее активен, замещение идет в положение 4, 8 и далее в 6.
Получение
- Из солей пиридиния [2]:

- По реакции 1,1-тиофендиоксида с диметиламинофульвеном[3]:

Применение
Азулен и, особенно, его природные производные достаточно широко используются в парфюмерии и косметике: входят в состав зубных паст, кремов, шампуней и других средств ухода за телом.
Физиологическая роль
Азулены обладают противовоспалительной, антиаллергенной и бактериостатической активностью, на чем и основано их применение.
Примечания
Ссылки
Углеводороды Алканы Метан • Этан • Пропан • Бутан • Пентан • Гексан • Гептан • Октан • Нонан • Декан • Ундекан • Додекан • Тридекан • Тетрадекан • Гексадекан • Эйкозан ... Алкены Этилен • Пропен • Бутен • Пентен • Гексен • Гептен • Октен ... Алкины Ацетилен • Пропин • Бутин Диены Пропадиен • Бутадиен • Изопрен Другие ненасыщеные Винилацетилен • Диацетилен Циклоалканы Циклопропан • Циклобутан • Циклопентан • Циклогексан • Декалин • Индан Ароматические Бензол • Толуол • Диметилбензолы • Этилбензол • Пропилбензол • Кумол • Стирол • Фенилацетилен • Индан • Циклобутадиен • Дифенил • Дифенилметан • Трифенилметан • Тетрафенилметан Полициклические Нафталин • Антрацен • Пентацен • Фенантрен • Пирен • Бензпирен • Азулен • Хризен Категории:- Полициклические ароматические углеводороды
- Косметические вещества
Wikimedia Foundation. 2010.