- Фторид никеля(II)
-
Фторид никеля(II) 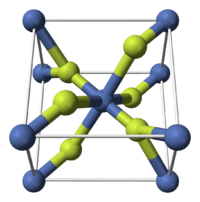
Общие Систематическое наименование фторид никеля(II) Традиционные названия фтористый никель Химическая формула NiF2 Физические свойства Состояние (ст. усл.) зеленовато-жёлтые кристаллы Молярная масса 96,69 г/моль Плотность 4,63 г/см³ Термические свойства Температура плавления 1027; 1163; 1452 °C Температура кипения субл. >1000; 1474; 1627 °C Молярная теплоёмкость (ст. усл.) 64,1 Дж/(моль·К) Энтальпия образования (ст. усл.) -658 кДж/моль Химические свойства Растворимость в воде 2,5620; 2,5890 г/100 мл Классификация Рег. номер CAS 10028-18-9 Рег. номер PubChem 24825 SMILES F[Ni]F Регистрационный номер EC 233-071-3 RTECS QR6825000 Фторид никеля(II) — неорганическое соединение, соль металла никеля и плавиковой кислоты с формулой NiF2, зеленовато-жёлтые кристаллы, хорошо растворяется в воде, образует кристаллогидрат.
Содержание
Получение
- Реакция никеля и фтора:
- Реакция хлорида никеля(II) и фтора:
Физические свойства
Фторид никеля(II) образует зеленовато-жёлтые кристаллы тетрагональной сингонии, пространственная группа P 4/mnm, параметры ячейки a = 0,471 нм, c = 0,3118 нм, Z = 2.
Образует кристаллогидраты состава NiF2•n H2O, где n = 2, 3, 4.
Из плавиковой кислоты выделен гидрат состава NiF2•5HF•6H2O.
Плохо растворим в воде, этаноле, диэтиловом эфире.
Химические свойства
- Кристаллогидрат при нагревании теряет воду:
- Реагирует с щелочами:
- Иначе реакция идёт с растворами аммиака:
- Восстанавливается водородом:
- С фторидами щелочных металлов образует комплексные соли:
- С фторидами щелочных металлов и фтором образует соли гексафтороникеляты:
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1992. — Т. 3. — 639 с. — ISBN 5-82270-039-8
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 2-е изд., испр. — М.-Л.: Химия, 1966. — Т. 1. — 1072 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — 871 с.
Соединения никеляАмид никеля (Ni(NH2)2) • Антимониды никеля • Арсениды никеля • Ацетат никеля(II) (Ni(CH3COO)2) • Бромид никеля(II) (NiBr2) • Гидрид никеля (NiH2) • Гидроксид никеля(I) (NiOH) • Гидроксид никеля(II) (Ni(OH)2) • Дисульфид(2-) никеля(II) (Ni(S2)) • Иодид никеля(II) (NiI2) • Карбид никеля Ni3C • Карбонат никеля(II) NiCO3 • Метагидроксид никеля (NiO(OH)) • Нитрат никеля(II) (Ni(NO3)2) • Нитриды никеля • Оксалат никеля(II) (NiC2O4) • Оксид никеля(I) (Ni2O) • Оксид никеля(II) (NiO) • Оксид никеля(II,III) (Ni3O4) • Октакарбонилдиникель (Ni2(CO)8) • Сульфат никеля (NiSO4) • Сульфид никеля(II) (NiS) • Тетракарбонилникель (Ni(CO)4) • Тетрацианоникколат(II) калия (K2[Ni(CN)4]) • Тиоцианат никеля(II) (Ni(SCN)2) • Титанат никеля(II) (Ni2TiO4) • Трицианоникелат(I) калия (K2[Ni(CN)3]) • Фосфат никеля(II) (Ni3(PO4)2) • Фосфиды никеля • Фторид никеля(II) (NiF2) • Хлорид гексаамминникеля(II) ([Ni(NH3)6]Cl2) • Хлорид никеля(II) (NiCl2) • Хромат никеля(II) (NiCrO4)• Цианид никеля(II) (Ni(CN)2)
 Категории:
Категории:- Соединения никеля
- Фториды
Wikimedia Foundation. 2010.






![\mathsf{NiF_2 + 6(NH_3\cdot H_2O) \ \xrightarrow{}\ [Ni(NH_3)_6]F_2 + 6H_2O }](c4ee42fa14add4c334153d4c3051cdb1.png)


![\mathsf{2NiF_2 + 6NaF + F_2 \ \xrightarrow{600^oC}\ 2Na_3[NiF_6] }](43fbb0b9b5c7a57cf7a057d9206ed4e3.png)