- Персульфид водорода
-
Персульфид водорода 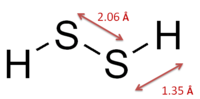
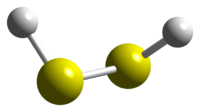
Общие Систематическое наименование диводород дисульфид Химическая формула H2S2 Физические свойства Состояние (ст. усл.) жёлтая жидкость Молярная масса 66,146±0,01 г/моль Плотность (при 25 °C) 1,3279 г/см³ Термические свойства Температура плавления -89.6 °C Температура кипения (344 K, 159 °F) 70.7 °C Классификация Рег. номер CAS 13465-07-1 SMILES SS Персульфид водорода — неорганическое бинарное химическое соединение водорода и серы. Химическая формула
 .
.Содержание
Структура
Структура персероводорода аналогична перекиси водорода: два центральных атома серы и два внешних атома водорода. Связь в соединении H—S—S имеет почти стандартный двугранный угол в 90°.
Косой угол в молекуле H2S2 составляет 90,6°, по сравнению с 113,7° у H2O2. Молекулярная длина между двумя атомами:
O—O, O—H, S—S и S—H равна 1,490, 0,970, 2,055 и 1,352 ангстрем соответственно[1][2].Синтез и реакции
Персульфид водорода может быть получен путем растворения полисульфидов щелочных или щелочноземельных металлов в воде. При смешивании с концентрированной соляной кислотой при температуре от −15 °C, желтое масло, состоящее из смеси полисульфанов (H2Sx, где x>1) будет оседать ниже водного слоя. Фракционированная конденсация этого масла позволит выделить персульфид водорода отдельно от других полисульфидов (в основном от трисульфида)[3][4].
Персульфид водорода легко разлагается при температуре окружающей среды до сероводорода и серы[4]:
В органической химии, персульфид водорода добавляют в алкены, что бы получить дисульфиды и тиолы[5].
Влияние на здоровье
Персульфид водорода был описан как «имеющий раздражающий запах», который похож на камфору или хлориды серы, вызывает «слезоточивость и жгучее ощущение в носу»[4]. Если он присутствует в высокой концентрации, то может вызваться головокружение, дезориентация и в конечном счете беспамятство[6].
Примечания
- ↑ Davies, D. W. Photoelectron spectra of hydrogen peroxide and hydrogen disulfide: ab initio calculations. — Chemical Physics Letters, 1974. — С. 520–522. — DOI:10.1016/0009-2614(74)80093-X
- ↑ P. Lazzeretti и R. Zanasi On the calculation of parity-violating energies in hydrogen peroxide and hydrogen disulfide molecules within the random-phase approximation. — Chemical Physics Letters, 1997. — В. 279. — С. 349–354. — DOI:10.1016/S0009-2614(97)01060-9
- ↑ De, A. K. A Text Book of Inorganic Chemistry. — ISBN 9788122413847
- ↑ 1 2 3 Walton и Parson Preparation and Properties of the Persulfides of Hydrogen. — J. Amer. Chem. Soc., 1921. — В. 43. — С. 2539–48. — DOI:10.1021/ja01445a008
- ↑ Hazardous Reagents, Robinson Brothers
- ↑ Stein, Wilkinson, G Seminars in general adult psychiatry. — Royal College of Psychiatrists, 2007. — ISBN 9781904671442
Категории:- Соединения серы
- Соединения водорода
- Неорганические вещества
- Бинарные соединения
Wikimedia Foundation. 2010.

