- Оксид молибдена(VI)
-
Триоксид молибдена 
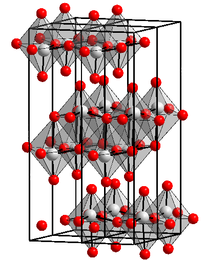
__ Mo6+ __ O2−
Общие Систематическое наименование Оксид молибдена(VI) Традиционные названия триоксомолибден, молибдит Химическая формула MoO3 Физические свойства Состояние (ст. усл.) жёлтый порошок Молярная масса 143.94 г/моль Плотность (тв., при 20 °C) 4.69[1] г/см³ Термические свойства Температура плавления 795 °C Температура кипения 1255 °C Молярная теплоёмкость (ст. усл.) 75,02[1] Дж/(моль·К) Энтальпия образования (ст. усл.) −745.17 кДж/моль Давление пара (734 °C) 1[1]
(797 °C) 10
(954 °C) 100Химические свойства Растворимость в воде (18 °C) 0.1066 г/100 мл
(70 °C) 2.055 г/100 мл
Структура Кристаллическая структура орторомбическая Классификация Рег. номер CAS 1313-27-5 Безопасность ЛД50 (крысы, орально) 125 мг/кг Оксид молибдена(VI) (триоксид молибдена, триоксомолибден, молибдит) — бинарное неорганическое химическое соединение кислорода с молибденом. Химическая формула
 . Это соединение производится в крупных масштабах из любого соединения молибдена. Это соединение используется в качестве сырья для производства металлического молибдена.
. Это соединение производится в крупных масштабах из любого соединения молибдена. Это соединение используется в качестве сырья для производства металлического молибдена.
Степень окисления молибдена в этом соединении равна +6.Содержание
Структура
В газовой фазе, три атома кислорода вместе связаны с центральным атомом молибдена. В твердом состоянии безводный
 состоит из слоев искаженных октаэдров
состоит из слоев искаженных октаэдров  в ромбической форме кристаллов. Края октаэдров образуют цепочки, которые соединены с атомами кислорода, которые и образуют слои. Октаэдры имеют один короткую связь O—Mo с несоединенным кислородом[2].
в ромбической форме кристаллов. Края октаэдров образуют цепочки, которые соединены с атомами кислорода, которые и образуют слои. Октаэдры имеют один короткую связь O—Mo с несоединенным кислородом[2].Свойства и получение
Слабо парамагнитные двулучепреломляющие белые орторомбические кристаллы слоистой структуры, желтеющие при нагревании[3]. Реагирует с кислотами, щелочами, раствором аммиака и сульфида натрия[1]. Растворяется в воде, в избытке растворов щелочей или карбонатов щелочных металлов. Триоксид молибдена производится промышленным методом обжига дисульфида молибдена — главной руды молибдена:
Получается прокаливанием молибдена на воздухе при высокой температуре:
Лабораторный синтез предполагает подкисление водного раствора молибдата натрия с хлорной кислотой[4]. При этом получаются диаква-триоксид молибдена и перхлорат натрия:
Диаква-триоксид молибдена легко теряет воду, давая моногидрат. Оба ярко-желтого цвета.
Молибденовый ангидрид растворяется в воде давая «молибденовую кислоту» (MoO3 · (2) H2O).Применение
Молибденовый ангидрид используется в производстве металлического молибдена, который служит как добавка в сталь и коррозионно-стойкие сплавы.
Влечет за собой соответствующие преобразования из MoO3 в реакции с водородом при повышенных температурах:
Кроме того, является со-катализатором для использования в промышленном производстве акрилонитрила путем окисления пропилена и аммиака.
Из-за своей слоистой структуры и благодаря свойству пары ионов MoVI/MoV данный оксид представляет интерес для использования в электрохимических устройствах и дисплеях[5].См. также
- Молибдит
Примечания
- ↑ 1 2 3 4 Молибдена (VI) оксид (рус.) 1. Архивировано из первоисточника 25 апреля 2012. Проверено 14 мая 2010.
- ↑ Wells, A.F. Structural Inorganic Chemistry. — Oxford: Clarendon Press, 1984. — ISBN 0-19-855370-6
- ↑ Важнейшие соединения молибдена (рус.).(недоступная ссылка — история) Проверено 14 мая 2010.
- ↑ Heynes, J. B. B.; Cruywagen, J. J. Yellow Molybdenum(VI) Oxide Dihydrate. — 1986. — С. 191. — (Inorganic Syntheses). — ISBN 0-471-83441-6
- ↑ Ferreira, F. F.; Souza Cruz, T. G.; Fantini, M. C. A.; Tabacniks, M. H.; de Castro, S. C.; Morais, J.; de Siervo, A.; Landers, R.; Gorenstein, A. Solid State Ionics. — 2000. — С. 136—137, 357.
Категории:- Соединения молибдена
- Бинарные соединения
- Неорганические вещества
- Соединения кислорода
Wikimedia Foundation. 2010.



